[ad_1]
 Datos de El ensayo CLARITY a principios de este año se suponía que sería la joya de la corona de la hipótesis amiloide, una reivindicación para los defensores de esta teoría de la enfermedad de Alzheimer sostenida por mucho tiempo pero muy difamada.
Datos de El ensayo CLARITY a principios de este año se suponía que sería la joya de la corona de la hipótesis amiloide, una reivindicación para los defensores de esta teoría de la enfermedad de Alzheimer sostenida por mucho tiempo pero muy difamada.
Sin embargo, los resultados hicieron que muchos se sintieran abrumados, e incluso los autores del estudio no se comprometieron.
La versión de prueba de CLARITY tiene muchas funciones excelentes. Reclutó a unas 1800 personas de todo el mundo, bastante equilibradas entre mujeres y hombres. Aunque la mayoría eran blancos, el 17 % de la cohorte era asiático y el 12 % hispano.
La selección de los resultados primarios y secundarios fue impecable. El resultado primario fue el CDR-SB (CDR-SB), un puntaje único calificado por un médico en los dominios de memoria, orientación, resolución de problemas, asuntos comunitarios, responsabilidades del hogar y cuidado personal. Los resultados secundarios incluyeron medidas estándar de funcionamiento cognitivo global, funcionamiento diario y biomarcadores cerebrales obtenidos del líquido cefalorraquídeo y la sangre.
¿Entonces qué pasó? Brevemente, el grupo de infusión de anticuerpo amiloide quincenal empeoró la CDR-SB en 1,21 puntos, mientras que el grupo de placebo empeoró en 1,66 puntos, una diferencia media de 0,45 puntos. Así es, ¡menos de medio punto para CDR-SB! Menos que el cambio más pequeño practicable a nivel individual y calculado solo comparando las medias de los grupos.
Al mismo tiempo, las exploraciones PET de los participantes mostraron una reducción significativa de amiloide. Se eliminó casi el 75% del amiloide fibrilar cerebral original; la mayoría de las personas pasan de amiloide «positivo» a amiloide «negativo». Aunque la eliminación de amiloide se ha visto en estudios anteriores con varios antiamiloides, este es el resultado biológico más convincente y es realmente difícil imaginar un mejor resultado de imágenes cerebrales.
una vez dicho esto el aspecto más preocupante fue la falta de un resultado estadísticamente significativo, por no hablar de un resultado clínicamente significativo, en mujeres para el resultado primario o secundario clínico (Figuras complementarias 1 a 4). En otras palabras, la lectura del titular fue impulsada por resultados positivos en los hombres, y es extremadamente sorprendente que esto no se haya discutido en el artículo. Esto no puede explicarse por un poder estadístico insuficiente y sugiere una interacción biológica más fundamental a nivel de eficacia terapéutica o mecanismo de acción. Esto necesita un análisis cuidadoso y más investigación para averiguarlo.
Recuerde que estos resultados «borrosos» implican poco o ningún riesgo de efectos secundarios. El 26 % de los que recibieron una dosis IV cada dos semanas tuvo una reacción a la infusión y el 21,5 % tuvo ARIA, una forma de anomalía en las imágenes cerebrales asociada con sangrado e inflamación que es común solo en aquellos que recibieron medicamentos antiamiloides. Aunque la mayoría son benignos, alrededor de una cuarta parte son clínicamente significativos, incluido el accidente cerebrovascular, y en cualquier caso, las anomalías de ARIA requieren un diagnóstico y tratamiento expertos.
En general, lecanemab es el antiamiloide más potente hasta la fecha pero, al igual que todos sus parientes terapéuticos, no ha logrado demostrar una diferencia clínicamente importante en comparación con el placebo, especialmente en las mujeres.
EN Carta al editor En el New England Journal of Medicine publicado hace unos días, el profesor Álvaro Pascual-Leone de Harvard y yo presentamos estas preocupaciones a la comunidad académica. Nuestra idea principal es simple. Parece haber un patrón recurrente en los datos del ensayo, según el cual los resultados clínicos son estadísticamente significativos para los hombres pero no para las mujeres.
A continuación se muestran los datos originales del artículo (Figura S1) para el criterio principal de valoración del ensayo, CDR-SB con mi anotación en rosa. Haga clic para expandir la imagen:
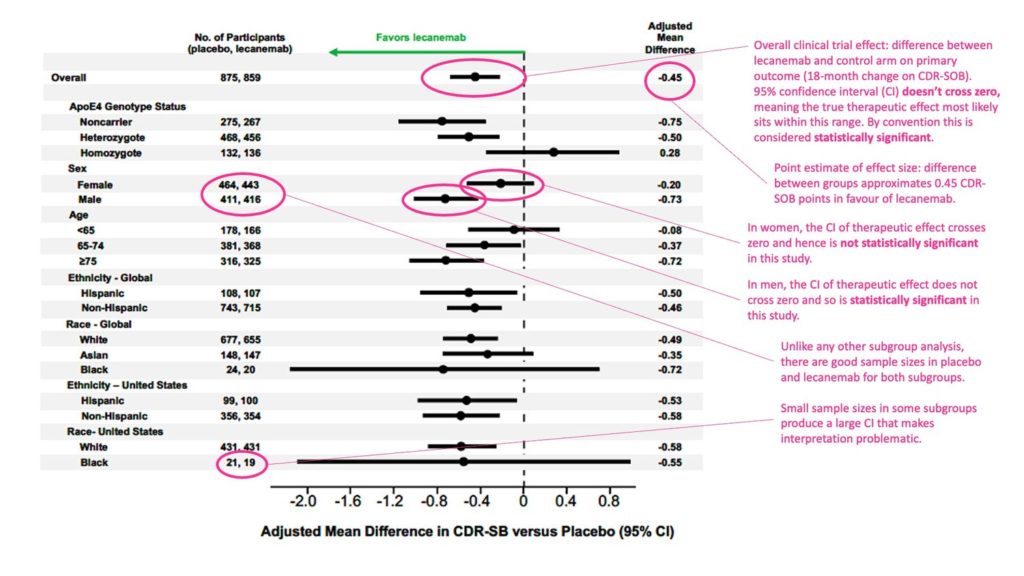
Para aquellos que no están acostumbrados a estas áreas forestales, si intervalo de confianza de una comparación particular cruza cero, entonces la diferencia entre los grupos se considera estadísticamente insignificante. Si el intervalo de confianza no cruza cero, la comparación es válida.
Claramente, para CDR-SB, el resultado fue estadísticamente significativo en los hombres (la diferencia calculada entre el tratamiento y el placebo fue de 0,73 puntos). También está claro que el resultado no fue significativo en las mujeres (diferencia media calculada de 0,20 puntos).
Sobre la base de este ensayo, se puede concluir que el efecto clínico general de lecanemab, como se informa a menudo (diferencia de puntos de 0,45 CDR-SOB), surge de un efecto terapéutico real, aunque débil, en los hombres, pero un efecto insignificante en las mujeres.
Si lecanemab no funciona en mujeres, es un gran problema. Desafortunadamente, la respuesta de los autores, publicada junto con nuestra Carta, no arroja luz sobre este tema.
Primero, argumentan que el ensayo carecía de la capacidad de analizar subgrupos individuales. Pero el análisis de subgrupos se planeó previamente de acuerdo con el protocolo publicado y, por lo tanto, los resultados de los subgrupos merecen consideración.
Una explicación para el resultado nulo en las mujeres es el error de muestreo, pero el tamaño de los subgrupos fue normal (n>400 para hombres y mujeres) y los autores aceptan al pie de la letra que las puntuaciones de las mujeres fueron más bajas que las de los hombres. Si va a interpretar estimaciones puntuales, ¿por qué no considerar también su grado de precisión, el intervalo de confianza?
La alternativa es que lecanemab no es realmente efectivo en las mujeres. Este aumento en las probabilidades, considerando resultados nulos en mujeres, también se observó en todos los demás criterios de valoración secundarios clínicos en Figuras S2-S4 (ADAS-COG14, ADCOMS, ACDS-MCI-ADL).
En segundo lugar, afirman que «el análisis de subgrupos muestra que lecanemab se desempeñó mejor que el placebo en todos los resultados clínicos, biomarcadores y calidad de vida de las mujeres, resultados que fueron consistentes con la eficacia general». Parece que están discutiendo sobre eso. cualquier la ventaja numérica en el grupo de tratamiento en mujeres es suficiente, independientemente de las estadísticas. Esto es inaceptable y potencialmente peligroso.
Francamente, si lecanemab no funciona en las mujeres, no sería ético ofrecerlo a las mujeres.
Recuerde que esta costosa inmunoterapia está asociada con riesgos significativos, incluida una alta incidencia de GRI e incluso la muerte. En la innovación biotecnológica, dicho riesgo puede aceptarse en el contexto de una probabilidad razonable de beneficio clínico y debe evitarse si esos beneficios son inciertos o desconocidos.
Desde un punto de vista científico, hay problemas adicionales. ¿Por qué no funciona para las mujeres? ¿Cuál es la base biológica de la decisiva influencia del género en el mecanismo de acción? ¿Y esto es específico de lecanemab o es un problema para toda la clase de antiamiloide?
Abordar estos problemas de una manera abierta y significativa ahora es fundamental para la credibilidad de este nuevo fármaco y, me atrevo a decir, de la industria en su conjunto.
 – Profesor Miguel Valenzuela es profesor invitado en el Centro para el Envejecimiento Cerebral Saludable de la Universidad de Nueva Gales del Sur, Australia, miembro del Consorcio Clínico sobre Envejecimiento Saludable de la Organización Mundial de la Salud y cofundador y director ejecutivo de Skin2Neuron Pty Ltd. Este artículo es una combinación editada de dos de sus publicaciones de blog anteriores en www.piel2neuron.org.
– Profesor Miguel Valenzuela es profesor invitado en el Centro para el Envejecimiento Cerebral Saludable de la Universidad de Nueva Gales del Sur, Australia, miembro del Consorcio Clínico sobre Envejecimiento Saludable de la Organización Mundial de la Salud y cofundador y director ejecutivo de Skin2Neuron Pty Ltd. Este artículo es una combinación editada de dos de sus publicaciones de blog anteriores en www.piel2neuron.org.
Noticias en contexto:
[ad_2]
Source link





